Universitäre Qualifikation
Die größte Fakultät für Medizin der Welt"
Präsentation
Informieren Sie sich über die Bereiche der onkologischen Verdauungschirurgie, in denen in den letzten Jahren die größten Fortschritte erzielt wurden, einschließlich ergänzender Studien und fortschrittlicher chirurgischer Techniken“
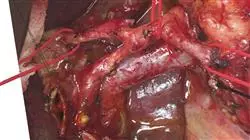
Die Entwicklungen und Meilensteine auf dem Gebiet der onkologischen Verdauungschirurgie haben es ermöglicht, den Pflegestandard erheblich zu verbessern. Multimodale Therapien wie die Polychemotherapie, die hochfokussierte Strahlentherapie oder die zielgerichteten molekularen Therapien haben die Handlungs- und Eingriffsmöglichkeiten der Fachärzte stark erweitert und zwingen sie ihrerseits zu einem nahezu kontinuierlichen Prozess der Aktualisierung und Erneuerung.
Daher müssen die notwendigen Kriterien entwickelt werden, um zu bestimmen, wann neue Technologien nützlich sein können und wie sie eingesetzt werden sollten, um den größtmöglichen Nutzen aus ihnen zu ziehen. Die Onkologische Verdauungschirurgie kann nicht als ein lineares Fachgebiet verstanden werden, sondern muss mit einer multidisziplinären Vision abgedeckt werden, die es dem Chirurgen ermöglicht, sich mit der Radiologie, der Endoskopie oder den Ernährungsabteilungen zu verbinden, um eine wirksamere Diagnose und Behandlung zu erhalten.
Angesichts dieser Situation hat TECH ein Dozententeam aus renommierten Experten für fortgeschrittene chirurgische Techniken zusammengebracht, um diesen privaten Masterstudiengang zu schaffen. Ziel ist es nicht, eine Sammlung von chirurgischen Techniken zusammenzustellen, sondern die Möglichkeiten der aktuellen Chirurgie, die sie umgebenden Spezialgebiete und die neuen Technologien zu untersuchen, die dem Spezialisten zur Behandlung von Tumoren des Verdauungssystems zur Verfügung stehen.
Dazu gehören Themen aus den Bereichen der ösophagogastrischen und kolorektalen onkologischen Chirurgie sowie die Analyse der neuesten wissenschaftlichen Erkenntnisse bei Lebertumoren, Lebermetastasen, mesenchymalen Tumoren und anderen spezifischen Pathologien im Bereich der Verdauungsonkologie. Der Forschungsaspekt wird nicht vernachlässigt, und auch der Innovation und Entwicklung auf diesem Gebiet wird Raum gewidmet.
Dies ist eine großartige akademische Gelegenheit, Ihr Wissen auf dynamische und effektive Weise zu aktualisieren und sich auf Ihre eigene klinische Praxis auf höchstem Niveau zu konzentrieren. Das Studienformat ist im Übrigen vollständig online. Das bedeutet, dass es keine Präsenzveranstaltungen und keine festen Stundenpläne gibt, so dass die Fachleute das Lehrpensum ganz flexibel an ihre eigenen Aufgaben anpassen können.
Vertiefen Sie Ihre Kenntnisse über das Management und die endoskopische Behandlung einer Vielzahl von Pathologien wie Speiseröhrenkrebs oder Gallengangstumoren“
Dieser Privater masterstudiengang in Onkologische Verdauungschirurgie enthält das vollständigste und aktuellste wissenschaftliche Programm auf dem Markt. Die wichtigsten Merkmale sind:
- Die Entwicklung von Fallstudien, die von Experten in Verdauungschirurgie und Onkologie vorgestellt werden
- Der anschauliche, schematische und äußerst praxisnahe Inhalt vermittelt alle für die berufliche Praxis unverzichtbaren wissenschaftlichen und praktischen Informationen
- Praktische Übungen, anhand derer der Selbstbewertungsprozess zur Verbesserung des Lernens verwendet werden kann
- Sein besonderer Schwerpunkt liegt auf innovativen Methoden
- Theoretische Lektionen, Fragen an den Experten, Diskussionsforen zu kontroversen Themen und individuelle Reflexionsarbeit
- Die Verfügbarkeit des Zugriffs auf die Inhalte von jedem festen oder tragbaren Gerät mit Internetanschluss
Sie können das gesamte didaktische Material herunterladen, um es später bequem von Ihrem Tablet, Smartphone oder Computer Ihrer Wahl aus zu studieren"
Zu den Dozenten des Programms gehören Experten aus der Branche, die ihre Erfahrungen in diese Fortbildung einbringen, sowie anerkannte Spezialisten aus führenden Gesellschaften und angesehenen Universitäten.
Die multimedialen Inhalte, die mit der neuesten Bildungstechnologie entwickelt wurden, werden der Fachkraft ein situiertes und kontextbezogenes Lernen ermöglichen, d. h. eine simulierte Umgebung, die eine immersive Fortbildung bietet, die auf die Ausführung von realen Situationen ausgerichtet ist.
Das Konzept dieses Programms konzentriert sich auf problemorientiertes Lernen, bei dem die Fachkraft versuchen muss, die verschiedenen Situationen aus der beruflichen Praxis zu lösen, die während des gesamten Studiengangs gestellt werden. Zu diesem Zweck wird sie von einem innovativen interaktiven Videosystem unterstützt, das von renommierten Experten entwickelt wurde.
Informieren Sie sich über den Einsatz von Big Data, künstlicher Intelligenz und neuronalen Netzen in der modernen Onkologieforschung"
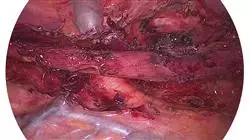
Legen Sie Ihren eigenen Zeitplan fest, denn der virtuelle Campus ist rund um die Uhr von jedem Gerät mit Internetanschluss aus zugänglich"
Lehrplan
Alle Inhalte dieses privaten Masterstudiengangs wurden auf der Grundlage der Relearning-Lehrmethodik entwickelt. Dies bedeutet, dass die akademische Erfahrung dynamischer und effektiver ist, da die Schlüsselkonzepte der onkologischen Verdauungschirurgie während des gesamten Programms wiederholt und auf natürliche Weise vermittelt werden. Dies spart wiederum eine beträchtliche Menge an Studienstunden, die zum Bestehen des Studiums erforderlich sind.
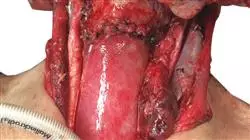
Greifen Sie auf detaillierte Videos, reale Fälle und praktische Analysen einer Vielzahl von häufigen und ungewöhnlichen Pathologien in der onkologischen Verdauungschirurgie zu“
Modul 1. Onkologische Verdauungschirurgie
1.1. Chirurgische Anatomie des Abdomens
1.1.1. Anatomie der Bauchhöhle
1.1.2. Anatomie des Ösophagogastriums
1.1.3. Hepatobiliäre Anatomie
1.1.4. Kolorektale Anatomie
1.2. Frührehabilitation. Multimodale Rehabilitation
1.2.1. Frührehabilitation
1.2.2. Intraoperative Maßnahmen
1.2.3. Postoperative Maßnahmen
1.3. Grundlagen der Ernährung in der onkologischen Verdauungschirurgie
1.3.1. Bestimmung des Ernährungszustandes
1.3.2. Folgen der Mangelernährung
1.3.3. Maßnahmen zur Verbesserung des präoperativen Ernährungszustandes
1.4. Anästhesie in der onkologischen Verdauungschirurgie
1.4.1. Vorbereitung auf die Anästhesie
1.4.2. Die Bedeutung der Anästhesie in der onkologischen Chirurgie
1.4.3. Anästhesie bei komplexen Eingriffen
1.5. Postoperative Wiederbelebung
1.5.1. Optimierung der Versorgung des Patienten nach der Operation
1.5.2. Erkennung von Frühkomplikationen
1.5.3. Sepsis und systemische Entzündungsreaktion
1.6. Palliative Chirurgie in der Onkologie der Verdauungsorgane
1.6.1. Was ist Palliation?
1.6.2. Wann sprechen wir von Palliation?
1.6.3. Palliative chirurgische Techniken
1.7. Grundlagen der Notfallchirurgie in der Verdauungsonkologie
1.7.1. Dringende Situationen in der onkologischen Chirurgie
1.7.2. Dringende ösophagogastrische Chirurgie
1.7.3. Dringende hepatobiliäre Chirurgie
1.7.4. Dringende kolorektale Chirurgie
1.8. Molekulare Grundlagen der Verdauungsonkologie
1.9. Wechselwirkung zwischen systemischen Behandlungen und Chirurgie
1.9.1. Wirkmechanismus der systemischen onkologischen Behandlungen
1.9.2. Wechselwirkung und Folgen für die Chirurgie
1.9.3. Maßnahmen zur Minimierung chirurgischer Komplikationen im Zusammenhang mit der systemischen Kontraktion
1.10. Strahlenonkologie in der onkologischen Verdauungschirurgie
1.10.1. Grundlegende Konzepte der Strahlentherapie
1.10.2. Prinzipien der Strahlentherapie in den verschiedenen Organen des Verdauungstraktes
1.10.3. Nebenwirkungen der Strahlentherapie auf den Gastrointestinaltrakt. Vorbeugung und Behandlung
Modul 2. Ergänzende Studien in der onkologischen Verdauungschirurgie
2.1. Die Rolle der konventionellen radiologischen Techniken
2.1.1. Erste Diagnose
2.1.2. Untersuchung der Ausdehnung bei Patienten mit Verdauungstumoren
2.1.3. Planung der Behandlung
2.2. Rolle der konventionellen Radiologie bei der Frühdiagnose und Nachsorge von Patienten mit Verdauungstumoren
2.2.1. Ultraschall
2.2.2. CT
2.2.3. MRT
2.3. Rolle der interventionellen Radiologie bei Verdauungstumoren
2.3.1. Diagnostische Techniken
2.3.2. Beteiligung an der Behandlung
2.3.3. Rolle bei der Behandlung von Komplikationen
2.4. Nuklearmedizin bei der Behandlung von Verdauungstumoren
2.4.1. Diagnostische Techniken
2.4.2. Rolle bei der Behandlung
2.4.3. Radiogesteuerte Chirurgie
2.5. Pathologische Diagnose. Jenseits des Morphologie
2.5.1. Bedeutung der intraoperativen Biopsie
2.5.2. Behandlung frischer Präparate und Untersuchung der Ränder
2.5.3. Histologische Risikofaktoren
2.5.4. Standardisierung von Berichten
2.6. Molekulare Diagnose
2.6.1. Konzept der molekularen Diagnostik
2.6.2. Krebs-Panels
2.6.3. Von der Diagnose zur Entwicklung personalisierter Therapien
2.7. Genetische Untersuchungen bei Patienten mit Risikofaktoren für Verdauungstumoren
2.7.1. Vererbte Syndrome, die mit Verdauungstumoren assoziiert sind
2.7.2. Erkennung von Risikopatienten
2.7.3. Nachsorge und prophylaktische Behandlung bei Risikopatienten
2.8. Endoskopie bei der Diagnose und Behandlung von Verdauungstumoren
2.8.1. Konventionelle und fortgeschrittene Endoskopie in der Diagnose
2.8.2. Einführung in endoskopische Techniken zur Behandlung von Verdauungstumoren
2.8.3. Endoskopie in der Palliativbehandlung
2.9. Mikrobiom und Verdauungstumoren
2.9.1. Konzept der Mikrobiota
2.9.2. Rolle des Mikrobioms bei der Karzinogenese
2.9.3. Rolle des Mikrobioms bei der Früherkennung und Prävention von Verdauungstumoren
2.10. Präoperative Beurteilung des älteren Patienten
2.10.1. Chirurgische Risikoskalen
2.10.2. Konzept der Fragilität
2.10.3. Prähabilitation bei älteren Menschen
Modul 3. Onkologische kolorektale Chirurgie
3.1. Kolorektaler Krebs
3.1.1. Epidemiologie und Ätiopathogenese
3.1.2. Diagnose und Stadieneinteilung
3.1.3. Nachsorge und Prognose des kolorektalen Adenokarzinoms
3.2. Polyposis-Syndrome
3.2.1. Diagnose
3.2.2. Behandlung
3.2.3. Follow-up
3.3. Endoskopische Behandlung von Vorläuferläsionen und frühem Krebs
3.3.1. Biliopankreatische Vorläuferläsionen
3.3.2. Früher Krebs
3.3.3. Entscheidungen nach endoskopischer Resektion
3.4. Chirurgische Behandlung von Dickdarmkrebs. Grundlegende Stomakonzepte
3.4.1. Rechter Dickdarm
3.4.2. Querkolon
3.4.3. Linker Dickdarm
3.4.4. Kolostomien und Ileostomien
3.5. Chirurgische Anatomie des Beckens
3.5.1. Allgemeine Konzepte
3.5.2. Männliches Becken
3.5.3. Weibliches Becken
3.6. Chirurgische Behandlung des Rektumkarzinoms
3.6.1. Frühe Phasen
3.6.2. Fortgeschrittene Stadien
3.6.3. Funktionelle Folgeerscheinungen
3.7. Medizinische Onkologie bei kolorektalem Krebs
3.7.1. Nicht metastasierendes kolorektales Karzinom
3.7.2. Metastasierendes kolorektales Karzinom
3.7.3. Palliative Behandlung
3.8. Onkologische Strahlentherapie bei kolorektalem Krebs
3.8.1. Strahlentherapie bei Rektumkarzinom
3.8.2. Strahlentherapie bei Rezidiv im Beckenbereich
3.8.3. Strahlentherapie in besonderen Situationen
3.9. Vollständige neoadjuvante Behandlung bei Rektumkarzinom. Watch and Wait
3.9.1. Konzept und Grundprinzipien der TNT
3.9.2. Aktuelle TNT-Schemata
3.9.3. Konzept des Watch and Wait, Handhabung und Hinweise
3.10. Chirurgische Behandlung in besonderen Situationen
3.10.1. Beckenrezidiv bei Rektumkarzinom
3.10.2. Positive pelvine Adenopathien bei Rektumkarzinom
3.10.3. Retroperitoneales Lymphknotenrezidiv: Chirurgie vs. Strahlentherapie
Modul 4. Onkologische ösophagogastrische Chirurgie
4.1. Allgemeine Aspekte von Speiseröhrenkrebs
4.1.1. Epidemiologie und Ätiopathogenese
4.1.2. Klassifizierung und Diagnose
4.1.3. Nachsorge und Prognose
4.2. Chirurgische Behandlung von Speiseröhrenkrebs
4.2.1. Arten der Anastomose
4.2.2. Standard- und erweiterte Lymphadenektomie
4.2.3. Alternativen zur Rekonstruktion mit Magenplastiken
4.3. Endoskopische und interventionelle Behandlung von Speiseröhrenkrebs
4.3.1. Behandlung von Vorläuferläsionen
4.3.2. Behandlung von Krebs im Frühstadium
4.3.3. Palliative Behandlung
4.3.4. Behandlung von Komplikationen
4.4. Krebs des ösophagogastrischen Übergangs
4.4.1. Kontroversen bei der Behandlung von AEG-Karzinomen
4.4.2. Ansatz nach neuen klinischen Leitlinien
4.4.3. Lymphadenektomie und chirurgischer Ansatz
4.5. Allgemeine Aspekte von Magenkrebs
4.5.1. Epidemiologie und Ätiopathogenese
4.5.2. Klassifizierung und Diagnose
4.5.3. Nachsorge und Prognose
4.6. Chirurgische Behandlung von Magenkrebs
4.6.1. Anastomose
4.6.2. Technische Grundlagen der Lymphadenektomie
4.6.3. Behandlung von Nicht-Adenokarzinom-Tumoren
4.6.4. Endoskopische Behandlung
4.7. Onkologische Therapien für Tumoren des Ösophagogastriums
4.7.1. Neoadjuvante und adjuvante Chemotherapie
4.7.2. Neoadjuvante und adjuvante Strahlentherapie
4.7.3. Neue onkologische Therapien: Immuntherapie
4.8. Komplikationen der onkologischen ösophagogastrischen Chirurgie
4.8.1. Postoperative Komplikationen
4.8.2. Post-Gastrektomie-Folgeerscheinungen
4.8.3. Post-Ösophagektomie-Folgeerscheinungen
4.9. Verbesserte Erholung bei ösophagogastrischer Chirurgie
4.9.1. Frührehabilitation
4.9.2. Optimierung
4.9.3. Klinische Pfade
4.10. Forschung und Innovation in der ösophagogastrischen onkologischen Chirurgie
Modul 5. Leber und Gallentrakt I. Allgemeines. Lebertumore
5.1. Chirurgische Anatomie der Leber
5.1.1. Hepatische Segmentierung
5.1.2. Hepatische Gefäßverteilung
5.1.3. Anatomie der Gallengänge
5.2. Diagnostische Tests in der hepatobiliären Pathologie
5.2.1. Ultraschall
5.2.2. CT
5.2.3. MRT
5.3. Bewertung von Restlebervolumen und -funktion
5.3.1. Konzept und Grenzen des Restlebervolumens
5.3.2. Techniken zur Messung des RLV
5.3.3. Methoden der Leberfunktionsbestimmung
5.4. Prinzipien der Leberchirurgie
5.4.1. Grundlagen und Stadien der Leberresektion
5.4.2. Techniken der Parenchymsektion
5.4.3. Pringle-Manöver und Gefäßkontrolle
5.4.4. Hämostase und Bilistase
5.5. Techniken zur Verbesserung der Resektabilität der Leber
5.5.1. Hepatische Regeneration
5.5.2. Portalembolisation und 2-stufige Operation
5.5.3. ALPPS-Technik
5.6. Minimalinvasive Leberchirurgie: Laparoskopie und Robotik
5.6.1. Grundlagen der minimalinvasiven Chirurgie in der hepatobiliären Chirurgie
5.6.2. Laparoskopischer Ansatz
5.6.3. Beitrag des robotergestützten Ansatzes
5.7. Komplikationen der Leberchirurgie und postoperatives Management
5.7.1. Postoperatives Management. ERAS
5.7.2. Komplikationen der hepatobiliären Chirurgie
5.7.3. Behandlung von Komplikationen
5.8. Gutartige und bösartige Lebertumore
5.8.1. Gutartige Lebertumore
5.8.2. Bösartige Lebertumoren
5.8.3. Hepatokarzinom: Epidemiologie, Risikofaktoren, Klassifizierung und Diagnose
5.9. Hepatokarzinom: Nichtchirurgische Behandlung
5.9.1. Alternative Behandlungen und „Brücken" zur Operation
5.9.2. Medizinische Behandlung
5.10. Hepatokarzinom: Chirurgische Behandlung
5.10.1. Untersuchung des Patienten mit Hepatokarzinom
5.10.2. Chirurgische Resektion
5.10.3. Lebertransplantation
Modul 6. Leber und Gallentrakt II. Tumoren des Gallentrakts. Lebermetastasen
6.1. Allgemeine Aspekte von Gallenblasen- und Gallengangskrebs
6.1.1. Epidemiologie und Ätiopathogenese
6.1.2. Klassifizierung
6.1.3. Diagnose
6.2. Chirurgie bei Tumoren des Gallenganges und der Gallenblase
6.2.1. Chirurgie von intrahepatischen Gallengangstumoren
6.2.2. Chirurgie bei extrahepatischen Tumoren der Gallenwege
6.2.3. Chirurgie von Gallenblasentumoren
6.3. Endoskopische und interventionelle Behandlung von Gallengangs- und Gallenblasentumoren
6.3.1. Präoperative endoskopische Behandlung
6.3.2. Präoperative interventionelle Radiologie
6.3.3. Endoskopisches Management von Komplikationen
6.3.4. Interventionelle Radiologie bei Komplikationen
6.4. Medizinisch-onkologische Behandlung von Gallengangs- und Gallenblasentumoren
6.4.1. Medizinische Onkologie bei Gallengangskrebs
6.4.2. Medizinische Onkologie bei Gallenblasenkrebs
6.5. Strahlenonkologische Behandlung von Gallengangs- und Gallenblasentumoren
6.5.1. Strahlentherapie bei Gallengangskrebs
6.5.2. Strahlentherapie bei Gallenblasenkrebs
6.6. Allgemeine Aspekte von Lebermetastasen
6.6.1. Epidemiologie und Ätiopathogenese
6.6.2. Klassifizierung
6.6.3. Diagnose und Prognose
6.7. Chirurgische Behandlung von Lebermetastasen bei kolorektalem Krebs und Alternativen zur chirurgischen Behandlung
6.7.1. Chirurgische Beurteilung und Planung bei Patienten mit Lebermetastasen von kolorektalem Krebs
6.7.2. Chirurgische Alternativen und Transplantation
6.7.3. Nichtchirurgische Alternativen
6.8. Medizinische Onkologie bei der Behandlung von Lebermetastasen bei kolorektalem Krebs
6.8.1. Neoadjuvante und adjuvante Behandlung
6.8.2. Palliative Behandlung
6.8.3. Neue Perspektiven
6.9. Metastasen von neuroendokrinen Tumoren
6.9.1. Klassifizierung, Diagnose und Prognose
6.9.2. Chirurgische Behandlung
6.9.3. Rolle der Lebertransplantation
6.10. Lebermetastasen von anderen nicht kolonektalen nicht neuroendokrinen Tumoren
6.10.1. Metastasen von HNO-Tumoren
6.10.2. Ösophagogastrische Tumor-Metastasen
6.10.3. Brustkrebs-Metastasen 1
6.10.4. Metastasierung von Bauchspeicheldrüsenkrebs
Modul 7. Pankreas, Zwölffingerdarm und Milz
7.1. Epidemiologie, Risikofaktoren und Genetik von Pankreaskarzinom.
7.1.1. Epidemiologie von Pankreaskarzinom
7.1.2. Risikofaktoren
7.1.3. Genetik
7.2. Diagnose von Pankreaskarzinom
7.2.1. Radiologie
7.2.2. Endoskopie
7.2.3. PET-CT
7.3. Therapeutische Strategie nach der NCCN-Klassifikation des Pankreaskarzinoms
7.3.1. Resektabler Tumor
7.3.2. Borderline-Tumor
7.3.3. Nicht resektabler Tumor
7.3.4. Metastasierender Tumor
7.4. Laparotomische Operationstechniken bei Bauchspeicheldrüsenkrebs
7.4.1. Kausch-Whipple-Operation
7.4.2. Distale Pankreatektomie
7.4.3. Zentrale Pankreatektomie
7.5. Minimalinvasive Techniken: Laparoskopie und Robotik bei Pankreaskarzinom
7.5.1. Laparoskopische Duodenopankreatektomie
7.5.2. Laparoskopische distale Pankreatektomie
7.5.3. Robotische Pankreaschirurgie
7.6. Palliative chirurgische Techniken bei Pankreaskarzinom
7.6.1. Palliation der Gelbsucht
7.6.2. Obstruktion der Verdauungsorgane
7.6.3. Schmerzkontrolle
7.6.4. Palliative ablative Techniken
7.7. Postoperative Komplikationen bei Pankreaskarzinom
7.7.1. Pankreasfistel
7.7.2. Verzögerte Magenentleerung
7.7.3. Postoperative Hämorrhagie
7.7.4. Biliäre Fistel
7.7.5. Sonstige Komplikationen
7.8. Chemotherapie und Strahlentherapie bei Pankreaskarzinom
7.8.1. Neoadjuvante
7.8.2. Adjuvans
7.8.3. Palliativmedizinische Behandlung
7.8.4. Strahlentherapie
7.9. Andere Tumoren der Bauchspeicheldrüse
7.9.1. Zystische Tumoren
7.9.2. Neuroendokrine Tumore
7.9.3. Seltene Tumoren des Pankreas
7.10. Zwölffingerdarm- und Milztumoren
7.10.1. Zwölffingerdarmtumoren
7.10.2. Milztumoren
Modul 8. Maligne Peritonealerkrankung
8.1. Grundsätze der Behandlung von malignen Peritonealerkrankungen
8.1.1. Pathophysiologie der peritonealen Ausbreitung. Mechanismen
8.1.2. Indikationen für radikale vs. Palliative Behandlung
8.1.3. Prognostische Faktoren
8.2. Bewertung der malignen Peritonealerkrankung
8.2.1. Prognostische Faktoren
8.2.2. Rolle der Laparoskopie
8.2.3. Histologische Klassifizierung
8.3. Zytoreduktive Chirurgie: Technik
8.3.1. Vorbereitung und Positionierung des Patienten
8.3.2. Verfahren der Peritonektomie
8.3.3. Kriterien für die Inoperabilität
8.4. Intraperitoneale Chemotherapie
8.4.1. Pharmakokinetische Grundlage
8.4.2. Modalitäten der intraperitonealen Chemotherapie: Indikationen und Anwendung
8.4.3. HIPEC-Technik
8.5. Neoplasmen des Blinddarms
8.5.1. Histologische Klassifizierung
8.5.2. Natürlicher Verlauf und Staging
8.5.3. Chirurgische Behandlung
8.6. Pseudomyxoma Peritonei
8.6.1. Definition und Epidemiologie
8.6.2. Histopathologische Klassifizierung und Prognose
8.6.3. Behandlung
8.7. Peritoneale Karzinomatose durch kolorektales Karzinom
8.7.1. Behandlung
8.7.2. Rolle des HIPEC
8.7.3. Frühdiagnose und Prävention
8.8. Peritoneale Karzinomatose aufgrund von Magenkrebs
8.8.1. Behandlung mit radikaler Absicht: Auswahl
8.8.2. Palliative Behandlung: intraperitoneale Optionen
8.8.3. Prävention
8.9. Peritoneale Karzinomatose aufgrund von Eierstockkrebs
8.9.1. Primärbehandlung
8.9.2. Rolle der HIPEC
8.9.3. Behandlung des Peritonealrezidivs
8.10. Peritoneal-Mesotheliom
8.10.1. Definition und Epidemiologie
8.10.2. Histopathologische Klassifizierung und Prognose
8.10.3. Behandlung
Modul 9. Mesenchymale Tumoren. Tumoren des Dünndarms
9.1. Epidemiologie, Diagnose und Klassifizierung von Weichteilsarkomen und retroperitonealen Sarkomen. Rolle der Biopsie
9.1.1. Epidemiologie
9.1.2. Klassifizierung
9.1.3. Diagnostische Methoden
9.1.4. Rolle der Biopsie
9.2. Grundsätze der Bildgebung bei mesenchymalen Tumoren.Die Rolle der Radiologie bei der Bewertung des Ansprechens auf die Behandlung
9.2.1. Mesenchymale Tumoren: allgemeiner Überblick
9.2.2. Weichteiltumore
9.2.3. Weichteiltumore: diagnostischer Ansatz
9.2.4. Weichteiltumore: im Detail
9.2.5. Retroperitoneale Sarkome
9.2.6. Mesenchymale Tumoren des Gastrointestinaltrakts
9.2.7. Gastrointestinale Stromatumoren (GIST)
9.2.8. Rolle der Radiologie beim Ansprechen auf die Behandlung und bei der Nachsorge von Nicht-GIST-Weichteilsarkomen
9.3. Chirurgische Behandlung von gastrointestinalen Stromatumoren (GIST). Radikale Chirurgie, minimalinvasive Chirurgie, Chirurgie bei Rezidiv, Chirurgie bei Metastasierung.
9.3.1. Inzidenz und Epidemiologie
9.3.2. Histologie und Molekularbiologe
9.3.3. Klinische Merkmale und diagnostischer Ansatz
9.3.4. Staging und RIisikofaktoren
9.3.5. Behandlung von lokoregionalen Erkrankungen
9.3.5.1. Radikale Operation
9.3.5.2. Anatomische Lokalisation und chirurgische Technik
9.3.5.3. Minimalinvasive Chirurgie
9.3.5.4. Indikationen für eine adjuvante Therapie bei lokalisierter Erkrankung
9.3.6. Behandlung der lokal fortgeschrittenen Erkrankung
9.3.7. Behandlung von residualer, rezidivierender oder metastasierter Erkrankung
9.3.8. Follow-up
9.4. Systemische Behandlung, Prognose und Genotypisierung von GISTs
9.4.1. Einführung
9.4.2. Molekularbiologie und Klassifizierung
9.4.2.1. SDH-Komplex-kompetente GIST mit Mutationen in KIT oder PDGFRA
9.4.2.1.1. KIT-Gen
9.4.2.1.2. PDGFRA-Gen
9.4.2.1.3. Therapeutische Konsequenzen bei lokalisierter und fortgeschrittener Erkrankung
9.4.2.2. GIST ohne KIT/PDGFRA-Mutationen und kompetentem SDH-Komplex
9.4.2.2.1. NF1-Mutationen
9.4.2.2.2. BRAF-Mutationen
9.4.2.2.3. NTRK-Mutationen
9.4.2.2.4. Mutationen in FGFR
9.4.2.2.5. Andere seltene Mutationen
9.4.3. GIST mit SDH-Komplex-Mangel
9.4.4. Histopathologie von GIST
9.4.5. Lokalisierte Erkrankung und Risikostratifizierung
9.5. Retroperitoneale Sarkome. Grundsätze der systemischen und strahlentherapeutischen Behandlung
9.5.1. Einführung
9.5.2. Inhalt
9.5.3. Neoadjuvante/präoperative Therapie
9.5.3.1. Strahlentherapie
9.5.3.2. Chemotherapie
9.5.3.3. Hyperthermie
9.5.4. Intraoperative Strahlentherapie
9.5.5. Adjuvante/postoperative Therapie
9.5.5.1. Strahlentherapie
9.5.5.2. Chemotherapie
9.5.6. Empfehlungen von den Experten
9.5.6.1. National Comprehensive Cancer Network (NCCN)
9.5.6.2. Europäische Gesellschaft für Medizinische Onkologie (ESMO)
9.5.6.3. Transatlantische Task Force für Retroperitoneale Sarkome (TARPSWG)
9.5.7. Follow-up
9.6. Chirurgische Behandlung von retroperitonealen Sarkomen
9.6.1. Einführung
9.6.2. Chirurgie des retroperitonealen Liposarkoms
9.6.2.1. Grundlagen der Kompartmentchirurgie
9.6.2.2. Chirurgische Technik der Kompartmentchirurgie
9.6.3. Chirurgie bei anderen retroperitonealen Sarkomen
9.6.4. Chirurgische Handhabung von Rückfällen
9.7. Weichteilsarkome der Extremitäten und der Brustwand
9.7.1. Einführung
9.7.1.1. Klassifizierung
9.7.1.2. Inzidenz, Lokalisierung und Risikofaktoren
9.7.2. Diagnose
9.7.2.1. Lokale Untersuchung
9.7.2.2. Ergänzende Tests
9.7.3. Histologische Diagnose
9.7.3.1. Grad
9.7.3.2. Histologie
9.7.3.3. Stadieneinteilung des Tumors
9.7.4. Therapeutische Behandlung
9.7.4.1. Lokalisierte Erkrankung
9.7.4.1.1. Chirurgie
9.7.4.1.2. Strahlentherapie
9.7.4.1.3. Chemotherapie
9.7.4.1.4. Isolierte Gliedmaßenperfusion
9.7.5. Metastasierende Krankheit
9.7.5.1. Follow-up
9.8. Dünndarm- und Mesenterialtumoren. Neuroendokrine Tumoren des Gastrointestinaltrakts
9.8.1. Klassifizierung
9.8.2. Adenokarzinom des Dünndarms
9.8.2.1. Pathogenese, Risikofaktoren und prädisponierende Bedingungen
9.8.2.2. Stadieneinteilung und Prognose
9.8.2.3. Klinische Merkmale
9.8.2.4. Diagnose
9.8.2.5. Behandlung
9.8.3. Lymphome
9.8.3.1. Klinische Merkmale
9.8.3.2. Diagnose
9.8.4. Neuroendokrine Tumoren des Gastrointestinaltrakts
9.8.4.1. Klassifizierung und Nomenklatur
9.8.4.2. Inzidenz und Epidemiologie
9.8.4.3. Anatomie und Pathogenese
9.8.4.4. Klinisches Bild
9.8.4.5. Diagnose
9.8.4.6. Staging und RIisikofaktoren
9.8.4.7. Chirurgische Behandlung
9.8.4.8. Medizinische Behandlung
9.8.4.9. Follow-up
9.9. Desmoid-Fibromatose. Rolle der Molekularbiologie, der Strahlentherapie, der Chemotherapie und des „Watch and Wait“
9.9.1. Einführung
9.9.2. Molekularbiologie
9.9.3. Strahlentherapie
9.9.4. Chemotherapie
9.9.5. Watch and Wait
9.10. Chirurgie bei metastasierender Erkrankung bei mesenchymalen Tumoren
9.10.1. Chirurgische Behandlung pulmonaler Metastasen
9.10.2. Chirurgische Behandlung von Lebermetastasen
9.10.3. Chirurgische Behandlung von Peritonealmetastasen
9.10.3.1. Rolle der HIPEC-Therapie bei peritonealer Sarkomatose
9.10.3.1.1. Peritoneale Sarkomatose uterinen Ursprungs
9.10.3.1.2. Peritoneale Sarkomatose retroperitonealen Ursprungs
9.10.3.1.3. Peritoneale Sarkomatose sekundär zu GISTs
Modul 10. Innovation, Forschung und Entwicklung in der onkologischen Verdauungschirurgie
10.1. Grundlagenforschung in der chirurgischen Onkologie
10.1.1. Einführung der Genomik
10.1.2. Einführung in die Proteomik
10.1.3. Einführung in die Zytometrie
10.2. Plattformen zum Testen neuer Therapien
10.2.1. Tiermodelle
10.2.2. 2D-Zellbasierte Modelle
10.2.3. 3D-Organoid-Modelle
10.3. Klinische Forschung in der chirurgischen Onkologie
10.3.1. Gestaltung klinischer Studien
10.3.2. Finanzierungsquellen
10.3.3. Einführung in die Methodik der Zuschussbeantragung
10.4. Big Data, künstliche Intelligenz und der Einsatz neuronaler Netze in der onkologischen Forschung
10.4.1. Einführung in Big Data
10.4.2. Künstliche Intelligenz in der onkologischen Chirurgie
10.4.3. Einsatz von neuronalen Netzen in der Krebsforschung
10.5. Techniken und Anwendungen der Fluoreszenz in der fortgeschrittenen onkologischen Chirurgie
10.5.1. Einsatz der Fluoreszenz in der onkologischen Chirurgie
10.5.2. Techniken der Anwendung, Dosen, Zeiten
10.5.3. Ergebnisse
10.6. Navigationssysteme, 3D-Modelle und intraoperative virtuelle Realität bei der Behandlung onkologischer Erkrankungen
10.6.1. Navigationssysteme
10.6.2. Nützlichkeit und Anwendung von 3D-Modellen
10.6.3. Intraoperative virtuelle Realität
10.7. Minimalinvasiver Ansatz in der komplexen onkologischen Chirurgie
10.7.1. Konzept und Modalitäten des minimalinvasiven Ansatzes
10.7.2. Beschreibung der verschiedenen Modalitäten
10.7.3. Robotik
10.8. Intraoperative ablative und adjuvante Techniken in der Krebschirurgie
10.8.1. Intraoperative ablative Techniken: Wirkmechanismus
10.8.2. Unterschiede, Vorteile und Nachteile
10.8.3. Intraoperative Strahlentherapie
10.9. Flüssigbiopsie und zirkulierende DNA als diagnostische und prognostische Methoden bei fortgeschrittenen neoplastischen Erkrankungen
10.9.1. Was ist eine Flüssigbiopsie?
10.9.2. Wie wird eine Flüssigbiopsie durchgeführt?
10.9.3. Anwendungen der Flüssigbiopsie
10.10. Neue Wege der Krebsbehandlung
10.10.1. Target Therapy in der Verdauungsonkologie und bei Sarkomen
10.10.2. Immuntherapie bei Verdauungstumoren
10.10.3. CAR-T-Therapie
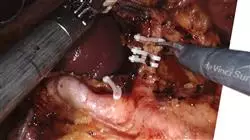
Laden Sie alle Inhalte herunter, um ein unverzichtbares Nachschlagewerk auf dem Gebiet der onkologischen Verdauungschirurgie zu erhalten, das auch nach Abschluss des Programms nützlich ist“
Privater Masterstudiengang in Onkologische Verdauungschirurgie
Entdecken Sie den Weg zur Exzellenz im Bereich der onkologischen Verdauungschirurgie mit unserem Privaten Masterstudiengang in Onkologische Verdauungschirurgie an der TECH Technologischen Universität. Wir bieten Ihnen die Möglichkeit, sich in diesem wichtigen Bereich der Medizin zu spezialisieren und ein international anerkannter Experte zu werden. Unser Online-Unterricht gibt Ihnen die Flexibilität, von jedem Ort und zu jeder Zeit zu studieren, die für Sie günstig ist. Sie müssen sich keine Gedanken über Pendeln oder feste Termine machen, da Sie bequem von zu Hause aus auf hochwertige Inhalte zugreifen und eine erstklassige Ausbildung erhalten können. In unserem Privaten Masterstudiengang in Onkologische Verdauungschirurgie werden Sie in das modernste und aktuellste Wissen über die Diagnose, Behandlung und Überwachung onkologischer Erkrankungen des Verdauungssystems eintauchen. Sie werden von anerkannten Experten auf diesem Gebiet unterrichtet, die Sie während des gesamten Programms anleiten werden, um die notwendigen Fähigkeiten zu erwerben und eine umfassende Vision der onkologischen Verdauungschirurgie zu entwickeln.
Nutzen Sie die besten Professoren bei TECH und bringen Sie Ihre Karriere auf den neuesten Stand
Profitieren Sie von unserer innovativen Lehrmethodik, die Theorie und Praxis durch echte klinische Fälle und interaktive Simulationen miteinander verbindet. Darüber hinaus haben Sie Zugang zu modernsten Multimedia-Ressourcen und einer virtuellen Lernplattform, die es Ihnen ermöglicht, mit Professoren und anderen Studenten zu interagieren und so den Austausch von Wissen und Erfahrungen zu fördern. Am Ende des Masterstudiengangs werden Sie darauf vorbereitet sein, sich den anspruchsvollsten Herausforderungen der onkologischen Chirurgie des Verdauungstrakts zu stellen und Ihren Patienten eine qualitativ hochwertige Behandlung anzubieten, die auf den besten Praktiken und den neuesten Forschungsergebnissen beruht. Sie erhalten einen international anerkannten Abschluss der TECH Technologischen Universität, der Ihr Fachwissen untermauert und Ihnen neue berufliche Möglichkeiten in Krankenhäusern, Kliniken und Forschungszentren eröffnet. Verpassen Sie nicht die Gelegenheit, sich auf dem Gebiet der onkologischen Chirurgie des Verdauungstraktes zu profilieren! Schreiben Sie sich in unseren Privaten Masterstudiengang in Onkologische Verdauungschirurgie ein und erweitern Sie Ihren beruflichen Horizont.







